Опыты на крысах Шмэля и соавторов
Шмэль и соавторы (Schmahl е. а., 1972) вызывали у крыс БП карциномы мочевого пузыря, нитроза метилмочевиной — гепатомы, а ДМБА — опухоли молочных желез.
Аппликация кожи мышей или пероральное введение крысам ретинилпальмитата либо ретиноевой кислоты не оказывали влияния на развитие опухолей.
Сирийским хомячкам интратрахеально в течение 12 недель вводили по 3 мг БП в сочетании с железняком (F2O3).
Затем в желудок вводили разные дозы ретинилацетата, который ускорял развитие опухолей дыхательных путей. При этом еженедельное поступление в организм 2,4 мг витамина сильнее стимулировало канцерогенез, чем доза в 0,1 мг (Smith, е. а., 1975). В другой работе эти же авторы указывают на коканцерогенный эффект витамина А в эпителии легких мышей при сочетанном действии с MX (Smith e. a., 1972).
Высокий уровень витамина А (500 мкг/г рациона) не изменял частоты выхода опухолей кишечника у крыс Спрейг-Доули; индуцированных внутрижелудочным введением ДМГ (Rogers е. а., 1973).
Причину коканцерогенного эффекта Спорн и соавторы (Sporn е. а., 1976) связывают с токсическим действием больших доз эфирных форм ретинола. При введении в желудок последние поступают в печень, где могут накапливаться и оказывать неблагоприятное действие на организм. Депонирование эфирных форм ретинола может не коррелировать с их содержанием в крови лабораторных животных.
Из природных витаминов антиканцерогенный эффект чаще всего проявлялся у самого, ретинола и ретиноевой кислоты, отличающихся по структуре только наличием спиртовой или карбоксильной групп. Ретиноевая кислота тоже токсична, но в отличие от эфирных форм не накапливается в печени.
В связи с неблагоприятным действием на организм трудно рассчитывать на длительное введение животным натуральных витаминов, а при кратковременном их использовании можно не достичь торможения канцерогенеза.
Поэтому возникла идея использовать искусственно синтезируемые производные витамина А в целях химопрофилактики химического канцерогенеза (см. обзор: Sporn е. а., 1976).
Структура производных ретинола позволяет включением в их состав различных химических группировок создавать препараты разнообразного биологического действия.
Как видно из рисунка, молекула витаминов состоит из трех основных компонентов — углеводородного кольца, углеводородной боковой цепи и полярных концевых групп.
Химические группировки, образующие структурные аналоги
производных витамина А (ретиноидов) (Sporn e. a., 1976)
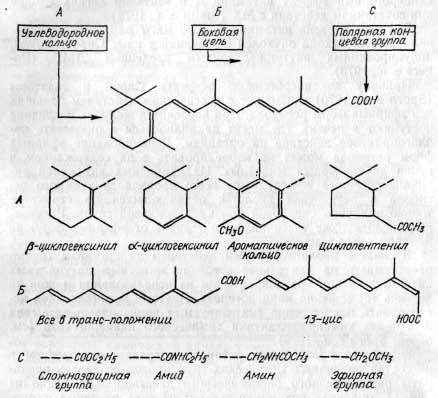
А, Б, С — возможные структуры соответственно углеводородных колец, боковых цепей и конечных групп.
Изменение в структуре каждого из этих компонентов приводит к новым проявлениям биологической активности.
Впервые исследования Боллаг (Bollag, 1974) показали, что замена циклогексинилового кольца ретиноевой кислоты ароматическим кольцом триметилметоксифенила, а концевой карбоксильной группы — этиловой, эфирной или этиламидной резко усиливает способность образующихся производных вызывать регрессию папиллом кожи мышей, индуцированных канцерогенами. Новые производные значительно менее токсичны, чем исходная ретиноевая кислота.
Это относится и к другому ее деривату — 13-цис-ретиноевой кислоте, которая, как показали Порт и соавторы (Port е. а., 1975), снижает частоту опухолей дыхательных путей у хомяков. Интратрахеальным введением небольших доз БП в сочетании с железняком вызывали опухоли — плоскоклеточные карциномы или карциномы in situ, которые образовались у 10% хомячков.
Другой группе животных после канцерогена каждую неделю вводили по 3 мг 13-цисретиноевой кислоты, и тогда опухоли возникли только у двух хомячков.
Увеличение дозы в 3 раза полностью предотвращало развитие опухолей. При этом не обнаруживали и токсического действия, хотя в тех же дозировках трансретиноевая кислота вызвала бы у животных резкую интоксикацию.
Спорн и соавторы (Sporn е. а., 1976) в своем обзоре указывают на возможность и других изменений в структуре витаминов, следствием которых могут быть новые биологические свойства. Так, ретинил-1Ч-ацетиламин оказывает влияние на процесс дифференцировки эпителия трахеи и при этом обладает слабой токсичностью. Альфа-ретинилацетат и альфа-ретиноевая кислота, в которых двойная связь в кольце изменена в положении 4 — 5 (на рисунке положение А), столь же активно, как бета-аналоги, контролируют дифференцировку эпителия трахеи.
Смотреть рисунок - Химические группировки, образующие структурные аналоги производных витамина А (ретиноидов) (Sporn e. a., 1976) (положение А)
Для биологической активности, по-видимому, не является обязательным наличие шестичленного углеводородного кольца — аналог, содержащий диметилацетилциклопентенил, также оказывает влияние на клеточную дифференцировку и подавляет процесс малигнизации, вызванный MX в культуре клеток простаты мышей (Lasnitzki, Goodman, 1974). По-видимому, возможны изменения в структуре боковой цепи витаминов, а также создание фторированных или хлорированных производных с нужными биологическими свойствами.
Решение этой задачи — дело будущего, но Спорн и соавторы (Sporn е. а., 1976) считают, что синтез новых биологически активных витаминов может быть столь же перспективным, как синтез стероидных гормональных препаратов, которые стали значительно полезнее для фармакотерапии, чем природные адренокортикоиды.
«Питание, канцерогены и рак»,
Б.Л. Рубенчик
Читайте далее:
